一位聪明的水手曾经告诉我关于船上电器的事:只要晚上灯亮,早上发动机启动,电动马桶冲水,一切都好,其他不紧急的事情可以等待。即使在我们的 40 英尺拖网渔船Bliss上实现电力涅槃所需的大量电池组,二十八年后的我仍然如此。然而不幸的是,我们今年早些时候对那个 1,855 安培小时的银行进行了烘烤,这意味着要进行极其昂贵的、未列入预算的更换,而且没有灯、没有发动机、没有厕所——一个真正的紧急情况。因此,在最近经历了选择过程之后,我想分享我对众多深循环高性能电池选择的了解。
在这个由两部分组成的系列中,我将探讨游艇上最常用的两种深循环船用电池技术的工作原理、选择标准和维护。第 1 部分介绍各种铅酸电池,第 2 部分将重点介绍锂离子技术。我的总体意图不是推荐特定的电池类型或制造商。与大多数与船有关的事情一样,选择电池时需要做出妥协,而且没有正确的答案。例如,Steve Dashew 在他的 FPB 781 Cochese上使用富液电池,Ben Ellison 在Gizmo上使用 Firefly 碳泡沫 AGM 电池,Ben Stein 希望在Have Another Day上尝试 Mastervolt LFP 锂离子电池,而我们已经使用了老式凝胶极乐细胞。您选择的电池将根据您船舶的具体需求而定,具体取决于价格、性能、容量、尺寸、重量、安装成本、充电方法、维护、预期寿命、安全考虑和安装位置等标准。
不幸的是,电池似乎有自己的想法。对于我们许多与他们住在一起的人来说,他们看起来喜怒无常,脾气暴躁,他们的日子有好有坏,而且似乎无法理解他们是如何工作的。大多数情况下,我们只是习惯了他们,并希望他们在我们需要时合作。为了了解如何最好地保养您的电池并选择最适合您的电池,我们需要深入研究铅酸和锂离子电池的化学成分。
让我们从老式铅酸电池开始,它已经存在了 100 多年。在此类别中,我们找到了富液式和密封式电池。水浸式电池有盖子,可以加水,而密封免维护电池则密封良好。密封电池,也称为阀控铅酸 (VRLA) 电池,分为三类,包括凝胶电解质(凝胶电池)、吸收玻璃垫 (AGM) 和碳泡沫 AGM。相同的化学原理适用于所有这些电池类型。它们的不同之处在于解决该技术固有的物理缺陷的方法。
了解铅酸电池的基本化学成分对于了解它们的工作原理以及如何保养它们非常有价值。但是,如果您一开始发现本节令人畏惧,那么在阅读下面更熟悉的主题之后阅读它可能会提高理解力。
铅酸电池具有以下基本组成部分:
在讨论电池时,术语“阳极”和“阴极”通常用于描述两极的极性(正或负)。不幸的是,相应的极取决于电池是否正在充电或放电。放电时,阳极指的是负极,阴极指的是正极。充电时,定义会切换,阳极为正极,阴极为负极。请注意,除非另有说明,否则在本文中,我们使用与阳极放电电池相关的术语,指的是负极。
在继续之前,让我讨论一些化学命名法,因为我们需要它来了解电池的工作原理。化学式中的字母代表氢(H)、硫(S)、氧(O)、铅(Pb)、锂(Li)、磷(P)和碳(C)等元素。这些组合成组以形成分子。分子可能具有一个或多个相同元素,由其字母指示符后面的小下标数字表示。因此,一个水分子(H 2 O)含有两个氢原子和一个氧原子。硫酸分子(H 2 SO 4)由2个氢、1个硫和4个氧原子组成。分子或原子前面的数字,如 2H 2O,对应于参与反应的分子数。最后,上标 + 或 – (如 H +)对应于实体的电荷。带电实体称为离子,中性实体称为原子或分子。因此,H 2 O是水分子,而SO 4 -2 是带有2个负电荷的硫酸根离子(即,其结构中具有两个额外的电子)。
电子 (e – ) 是带负电的粒子,将原子结合在一起形成分子。当自由电子(未与原子或分子结合的电子)流经电线时就会产生电流。
下图描述了电池放电和充电期间发生的电化学反应。阳极(负极)由铅(Pb)组成,阴极(正极)由氧化铅(PbO 2 )组成,电解质为硫酸((H 2 SO 4),介质或溶剂为水(H 2 O)。
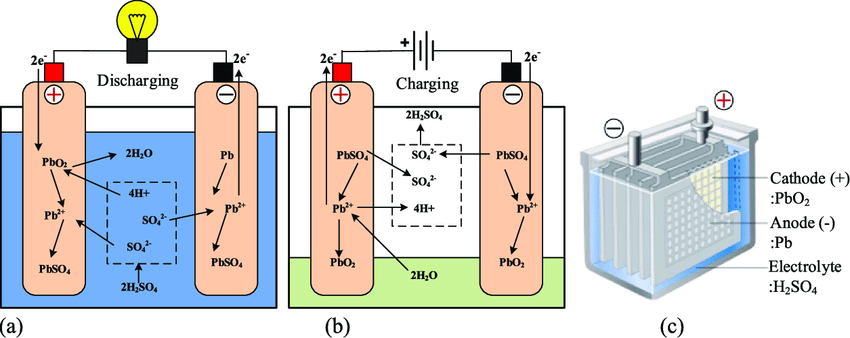
让我们首先看一下电池放电为船舶上的电子设备供电时发生的过程。在阳极(电池的负极),铅 (Pb) 释放 2 个电子和一个氢离子 (H + ),然后与硫酸根离子 (SO 4 -2 ) 结合形成硫酸铅 (PbSO 4)。在阴极,氧化铅 (PbO 2 ) 与 2 个电子、硫酸和阳极释放的游离氢离子 (H + ) 结合,形成硫酸铅 (PbSO 4 ) 和 2 个水分子 (H 2 O)。既然我们已经走到这一步了(几乎完成了),我们可以将其写为
阳极反应:Pb + HSO 4 – → PbSO 4 + H + + 2e –
阴极反应:PbO 2 + 3H + + HSO 4 – + 2e – → PbSO 4 + 2H 2 O
这里的关键要点是,阳极铅为我们提供了两个电子,这些电子穿过您的船进行电工作并最终到达阴极,从而产生水和硫酸铅。最后这句话很重要,因为它可以产生您所需的电力并影响电池的寿命(稍后会详细介绍)。
我不会花太多时间在电池充电上,这会颠倒操作。交流发电机会改变电流,导致电子从正极流向负极,在负极再生铅 (Pb),在正极再生氧化铅 (PbO 2 ) 。
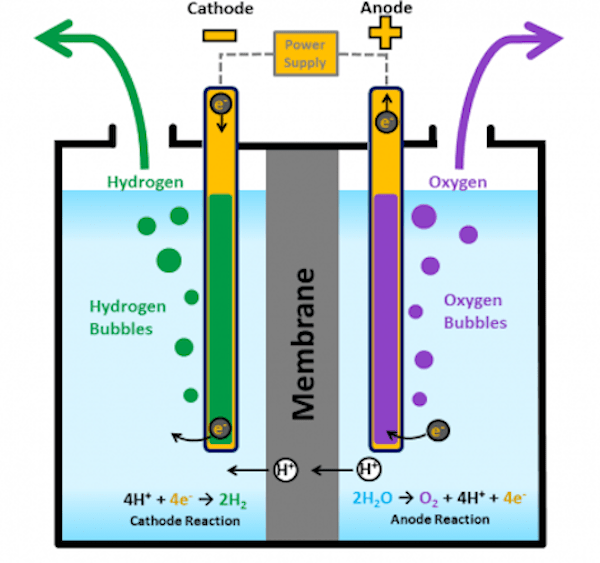
充电周期期间会发生不需要的(且不幸的)副反应。电流通过电解质会导致水分解成氢气 (H 2 ) 和氧气 (O 2 )。这个过程称为电解,在电池的负极释放氢气,在正极释放氧气。
恭喜!本节化学课结束。我们现在可以讨论反应的各个方面以及它们如何影响铅酸电池的操作和维护。
联系人:余工
手 机:198-5307-5821
邮 箱:batteryltd@sina.com