
锂离子电池中的正极材料是什么
电极是电池的核心,由活性物质和导电骨架组成。正负极活性物质是发电的源泉,是决定电池基本特性的重要组成部分。例如在锂离子电池中,目前商业化的锂离子电池正极活性物质一般为LiCoO 2,目前的科研热点正朝着无钴材料方向发展,市场上部分正极材料也使用LiMn 2 。 O 4等
电源内部的非静电力是单位正电荷通过内部电路从电源负极向正极移动过程中所做的功。电动势的符号是ℇ,单位是伏特(V)。电源是将其他形式的能量转换成电能的装置。要在电路中保持恒定电流,仅有静电场力是不够的,还要有非静电场力。电源提供非静电力,使正电荷从低电位移动到高电位。非静电力推动电荷做功的过程,就是其他形式的能量转化为电能的过程。
电动势是表征电源产生的电能的物理量。不同的电源具有不同的非静电力来源和不同的能量转换形式。例如化学电动势(干电池、纽扣电池、蓄电池、锂离子电池等)的非静电力是一种化学作用,电动势的大小与电池的大小无关电源;发电机的非静电力是磁场对运动电荷的作用力;光电动势(光电池)的非静电力来自内部光电效应;以及压电电动势(水晶压电打火机、水晶话筒等)
当电源的外部电路断开时,电源内部的非静电力与静电场力平衡,电源正负极两端的电压等于电源的电动势供应。当外电路导通时,端电压小于电动势。
对于锂离子电池,对活性物质的要求是:首先,电池的电动势高,即正极活性物质的标准电极电位越正,电池的标准电极电位越负。负极活性物质越多,电池的电动势越高。.
以锂离子电池为例。通常使用LiCoO 2作为正极活性物质,碳作为负极活性物质,可以获得高达3.6V以上的电动势;其次,活性物质的自发反应能力越好。电池的重量比容量和体积比大。LiCoO 2的理论重量比容量和石墨均较大,分别为279mA·h/g和372mA·h/g;此外,要求活性物质在电解液中具有较高的稳定性,以减少电池在储存过程中的自放电,从而提高电池的储存性能;此外,活性物质需要较高的电子导电率以降低其内阻;当然,从经济和环境的考虑,要求活性物质来源广泛,价格低廉,对环境友好。
除了上述要求外,锂离子电池正极活性材料的选择还有其特殊的要求。具体来说,锂离子电池正极材料的选择必须遵循以下原则。
①正极材料具有较大的吉布斯白能,从而与负极材料保持较大的电位差,提供电池工作电压(高比功率)。
②锂离子嵌入反应过程中吉布斯自由能变化ΔG小,即锂离子嵌入量大,电极电位对嵌入量的依赖性小,保证了稳定的工作电压锂离子电池。
③锂离子的嵌入/脱嵌范围广,锂离子的嵌入/脱嵌量相当大(比容量大)。
④正极材料需要有大孔“隧道”结构,以利于充放电过程中锂离子的嵌入/逸出。
⑤锂离子在“隧道”中具有较大的扩散系数和迁移系数,保证较大的扩散速率和良好的电子导电性,以提高锂离子电池的最大工作电流。
⑥正极材料界面结构大,结构更明显,增加放电时嵌锂的空间位置,提高其嵌锂容量。
⑦正极材料化学物理性能均匀,异常小,保证电池良好的可逆性(循环寿命长)。
⑧与电解液无化学或物理反应。
⑨ 与电解液相容性好,热稳定性高,确保电池工作安全。
⑩重量轻,易于制作合适的电极结构,提高锂离子电池的性价比。
⑪无毒、价格低廉、制备容易。
常用的正极活性物质除了LiCoO 2外,还有LiMn 2 O 4。
商用锂离子电池正极材料LiCoO 2属于α-NaFeO 2结构。层状岩盐钴酸锂的合成方法主要有高温固相法、低温共沉淀法和凝胶法。比较成熟的方法是高温固相法。
钴是一种战略元素。全球储量非常有限。它昂贵且有毒。因此,以LiCoO 2为正极活性物质的锂离子电池成本较高;另外,在LiCoO 2中,可逆脱嵌锂的量为0.5~0.6mol,当过充释放的锂大于0.6mol时,多余的锂以单质锂的形式沉积在负极上,也将带来安全隐患。LiCoO 2过充后生成的CoO 2对电解液氧化具有很强的催化活性。同时,CoO 2的初始分解温度温度低(240℃左右),放热量大(1000/g),所以用LiCoO 2作为锂离子电池的正极材料也存在严重的安全隐患,只适用于小容量单体电池单独使用。
与金属钴相比,金属镍便宜得多。世界已证明,镍的可采储量约为钴的14.5倍,毒性也较低。由于Ni和Co的化学性质接近,LiNiO 2和LiCoO 2具有相同的结构。两种化合物均属于α-NaFeO 2二维层状结构,适用于锂离子的脱嵌。LiNiO2没有过充过放的局限性,高温稳定性好,自放电率低,污染小,对电解液要求低。是一种很有前途的锂离子电池正极材料;然而,LiNiO 2在充放电过程中,其结构不稳定,制造工艺条件苛刻,不易制备出具有稳定α-NaFeO 2二维层状结构的LiNiO 2 。
LiNiO 2通常以LiOH、LiNO 3、Li 2 O、Li 2 CO 3等锂盐和Ni(OH) 2、NiNO 3、NiO等镍盐为原料,通过高温固相反应合成。. Ni与Li的摩尔比为(1:1.1)~(1:1.5),将反应物混合均匀后压制成片或丸,在650-850℃富氧气氛中煅烧5 -16 小时。
与钴酸锂和镍酸锂相比,锰酸锂具有良好的安全性和良好的抗过充能力。原料锰资源丰富、价格低廉、无毒,是最有发展前途的正极材料之一。锂锰氧化物主要有两种类型,即具有层状结构的LiMnO 2和具有尖晶石结构的LiMn 2 O 4 。
尖晶石LiMn 2 O 4属于立方晶系,空间群为Fd3m;其理论容量为148mA·h/g,其中氧原子形成面心立方密堆积(ccp),锂和锰分别占据ccp堆积的四面体位置。(8a)和八面体位置(16d),四面体晶格8a、48f和八面体晶格16c共面形成相互连通的三维离子通道,适合锂离子的自由脱嵌。
尖晶石LiMn 2 O 4的制备方法有高温固相法、熔盐浸渍法、共沉淀法、pechini法、喷雾干燥法、溶胶-凝胶法、水热合成等。
在充放电过程中,LiMn 2 O 4会发生从立方相到四方相的相变,导致严重的容量退化和低循环寿命。目前,研究人员通过掺杂其他半径和化合价与Mn相近的金属原子(Co、Ni、Cr、Zn、Mg等)来提高其电化学性能,效果明显。但一般来说,这些掺杂元素的加入量不宜过多,掺杂过多会明显降低电池的容量。其次,在化学计量的LiMn 2 O 4中加入过量的锂盐也可以提高其晶体结构的稳定性。
尖晶石LiM 2 O 4(M=Mn、Co、V等)中的M 2 O 4骨架是促进Li +扩散的四面体和八面体的共面三维网络。其典型代表是LiMn 2 O 4。由于在加热过程中容易失去氧气,产生电化学性能较差的缺氧化合物,因此高容量LiMn 2 O 4的制备较为复杂。尖晶石型,尤其是掺杂的LiMn2O4的结构与性能的关系,对于锂离子电池来说,还有待进一步研究。电极材料研究方向。
与LiCoO 2一样,层状LiMnO 2具有α-NaFeO 2的层状结构,理论容量为286mA·h/g。它在空气中稳定,是一种潜在的正极材料。其制备方法也多种多样。例如,高温固相法制备的层状LiMnO 2在2.5~4.3V充放电,可逆容量可达200mA·h/g。第一次充电后,正交晶系的 LiMnO 2将转变为尖晶石型。LiMn 2 O 4,所以可逆容量很差。
除了上述作为锂离子电池正极材料的过渡金属氧化物外,目前正在研究的热门正极材料还有多酸离子系LiMXO 4 、Li 3 M 2 ( XO 4 ) 3 (其中M = Fe, Co、Mn、V 等;X=P、S、Si、W 等)。
自1997年报道LiFePO 4中锂离子可逆脱嵌以来,具有有序结构的橄榄石型LiMPO 4材料受到广泛关注。美国的Valence已将类似材料应用到该公司的聚合电池中。
磷酸铁锂(LiFePO 4 )具有规则的橄榄石晶体结构,属于正交晶系(Pmnb)。每个单元电池中有四个 LiFePO 4单元。晶胞参数为 a=0.6008nm、b=1.0324nm 和 c=0.4694nm。
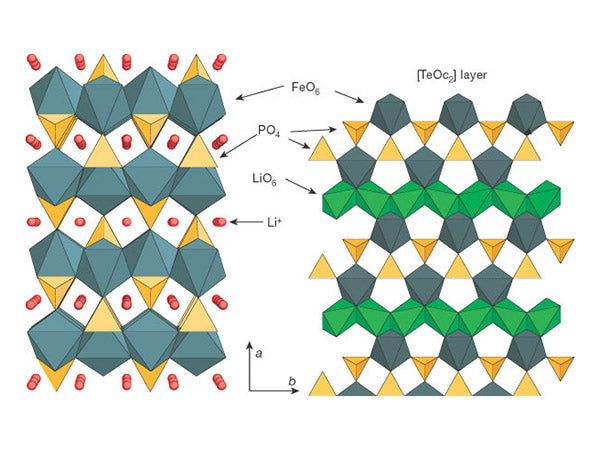
图1是LiFePO 4的三维结构示意图。
在LiFePO 4中,氧原子呈略微扭曲的六方密排排列,Fe和Li分别位于氧原子八面体的中心,形成FeO 6八面体和LiO 6八面体。FeO 6八面体、LiO 6八面体和PO 4四面体交替排列形成层状支架结构。在bc平面上,相邻的FeO 6八面体由一个共享顶点的氧原子相连,形成一个FeO6层。在 FeO6 层之间,相邻的 Li0 和八面体通过共享边缘的两个氧原子在 6 方向上连接形成链。每个 PO、四面体和 FeO 6八面体共享边上的两个氧原子,同时与两个LiO 6八面体共享边上的氧原子。
纯相LiFePO 4橄榄石的理论比容量为170mA·h/g,实际比容量可达160mA·h/g左右。稳定的橄榄石结构使LiFePO 4正极材料具有以下优点:
①更高的理论比容量和工作电压,1mol LiFePO 4可以脱嵌1mol锂离子,其工作电压约为3.4V(相对于Li+/Li);
②优异的循环性能,尤其是高温循环性能,提高使用温度也能提高其高倍率放电性能;
③安全性能优良;
④更高的振实密度(3.6mg/cm 3),更高的质量和体积能量密度;
⑤世界铁资源丰富,物美价廉,无毒。LiFePO 4被认为是环境友好的阴极材料。
尽管如此,LiFePO 4正极材料也有其缺点。该材料离子电导率低,Fe2+在合成过程中易氧化为Fe3+,需要相对纯净的惰性气氛保护等工作条件。目前,LiFePO 4研究的难点在于合成工艺困难,电极材料的高倍率充放电性能较差。
作为锂离子电池正极材料最基本的条件是在结构稳定的前提下,锂离子在电池充放电过程中可以从材料结构中可逆地脱嵌。许多磷酸盐具有类似于Na快离子导体(NASICON,钠超离子导体)的结构。在这类化合物中,有足够的空间传导Na+和Li+等碱金属离子,最重要的一点是化合物的结构比过渡金属氧化物稳定得多,即使在摩尔比Li +与过渡金属原子的比大于1。 Li 3 V 2 (PO 4 ) 3就是这样一个具有NASICON结构的化合物。
Li 3 V 2 (PO 4 ) 3是一种NASICON结构的化合物。该化合物有两种晶型,即三角/菱面体和单斜晶型,如图2(a)和(B)所示。
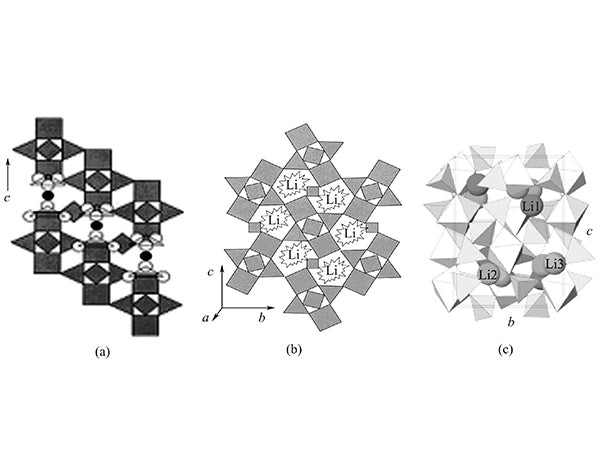
图2 Li 3 V 2 (PO 4 ) 3两种不同晶型的结构
在Li 3 V 2 (PO 4 ) 3中,PO4四面体VO 6通过共享顶点氧原子形成三维骨架结构。每个VO 6八面体周围有六个PO4四面体,每个PO4四面体周围有四个VO6八面体。这样,以A 2 B 3(其中A=VO 6,B=PO 4)为单元,形成三维网络结构。每个单晶由4个A2B3单元组成,晶胞中共有12个锂离子。图2(c)为单斜晶系Li 3 V 2 (PO 4) 3。
在以上两种晶型中,只有正交晶系是NASICON结构的化合物。在正交晶系Li 3 V 2 ( PO 4 ) 3中,A 2 B 3单元平行排列[图2(a)],而在单斜晶系Li 3 V 2 ( PO 4 ) 3排列成B形[图2(b)],减少了客体锂离子插入所占用的空间。这两种晶型都存在三相,主要是因为在不同的温度下有不同的相变。低温时为α相,中温时为β相,高温时为γ相。相之间的转变是可逆的。α-β和β-γ的相变只是由于锂原子在占据位置的分布。区别,尤其是β-γ相的转变,是从有序相到无序相的转变。Li 3 V 2 (PO 4 ) 3在120℃由α相转变为β相,在180℃由β相转变为γ相。
锂离子电池的正极通常混合有活性物质,如LiCoO 2、LiNixCo 1-x O 2或LiMn 2 O 4、导电剂(如石墨、乙炔黑)和粘合剂(如PVDF、PTFE)等,搅拌成糊状。,在铝箔两面均匀涂布,涂层厚度为15-20μm,在氮气流下吹干,去除有机分散剂,然后用辊压机压制成型,然后切成极片件按要求指定尺寸。
联系人:余工
手 机:198-5307-5821
邮 箱:batteryltd@sina.com